07年高考化学试题分类汇编——卤素
录入者:netlab 人气指数: 次 发布时间:2008年01月18日
66.(2007年高考广东文基,卤素)下列溶液能使红色花瓣快速褪色的是( )
(A)稀盐酸 (B)新制氯水
(C)氯化钙稀溶液 (D)生理盐水
[答案]B。
5.(2007年高考广东化学卷,卤素)氯气是一种重要的工业原料。工业上利用反应3Cl2+2NH3=N2+6HCl检查氯气管道是否漏气。下列说法错误的是( )
(A)若管道漏气遇氨就会产生白烟 (B)该反应利用了Cl2的强氧化性
(C)该反应属于复分解反应 (D)生成1 mol N2有6 mol电子转移
[答案]C。
31.(2007年高考广东理基,卤素)从海水可获得的在常温下为液体的单质是( )
(A)Mg (B)K (C)Br2 (D)I2
[答案]C。
4.(2007年高考广东化学卷,卤素)许多国家十分重视海水资源的综合利用。不需要化学变化就能够从海水中获得的物质是( )
(A)氯、溴、碘 (B)钠、镁、铝 (C)烧碱、氢气 (D)食盐、淡水
[答案]D。
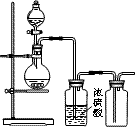
17.(2007年高考上海化学卷,卤素)可用如图装置制取(必要时可加热)、净化、收集的气体是( )
(A)铜和稀硝酸制一氧化氮 (B)氯化钠与浓硫酸制氯化氢
(C)锌和稀硫酸制氢气 (D)硫化亚铁与稀硫酸制硫化氢
[答案]B。
6.(2007年高考理综重庆卷,卤素)表中是食用碘盐包装上的部分说明,下列说法正确的是( )
|
配料 |
精盐、碘酸钾、抗结剂 |
|
碘含量 |
35±15 mg/kg |
|
储存方法 |
密封、避光、防潮 |
|
食用方法 |
烹饪时,待食品熟后加入碘盐 |
(A)高温会导致碘的损失 (B)碘酸钾可氧化氯化钠
(C)可用淀粉检验碘盐中的碘酸钾 (D)该碘盐中碘酸钾含量为20 mg/kg~50 mg/kg
[答案]A。
30.(2007年高考上海化学卷,卤素)一定量的氢气在氯气中燃烧,所得混合物用100 mL 3.00 mol/L的NaOH溶液(密度为1.12 g/mL)恰好完全吸收,测得溶液中含有NaClO的物质的量为0.0500 mol。
(1)原NaOH溶液的质量分数为 。
(2)所得溶液中Cl-的物质的量为 mol。
(3)所用氯气和参加反应的氢气的物质的量之比n(Cl2):n(H2)= 。
[答案](1)10.7%。 (2)0.25。 (3)3:2。
27.(卤素) (2007年高考全国理综卷II) (15分)现有五种离子化合物A、B、C、D和E,都是由下表中的离子形成的:
|
阳离子 |
Ag+ |
Ba2+ |
Al3+ |
|
阴离子 |
OH- |
Cl- |
SO42 - |
为鉴别它们,分别完成以下实验,其结果是:
(a) B和D都不溶于水,也不溶于酸;
(b) A溶于水后,与上述某阳离子反应可生成B,且A溶液与过量的氨水反应生成白色沉淀;
(c) C溶于水后,与上述某阳离子反应可生成D,且C溶液与过量的氨水过量反应生成白色沉淀;
(d) E溶于水后,与上述某阴离子反应可生成B;
(e) A溶液与适量E溶液反应生成沉淀,再加入过量E溶液,沉淀量减少,但不消失。
请根据上述实验结果,填空:
(1)写出化合物的化学式:A__________,C__________,D__________,E__________。
(2)A溶液与过量的E溶液反应后,最终得到的沉淀的化学式是____________。
[答案](1)Al2(SO4)3,AlCl3,AgCl,Ba(OH)2。 (2)BaSO4。
28.(2007年理综北京卷,卤素)(15分)北京市场销售的某种食用精制盐包装袋上有如下说明:
|
产品标准 |
GB5461 |
|
产品等级 |
一级 |
|
配料 |
食盐、碘酸钾、抗结剂 |
|
碘含量(以I计) |
20~50 mg/kg |
|
分装日期 |
|
|
分装企业 |
|
(1)碘酸钾与碘化钾在酸性条件下发生如下反应,配平化学方程式(将化学计量数填于空白处):
___KIO3+___KI+___H2SO4 =___K2SO4+___I2+___H2O
(2)上述反应生成的I2可用四氯化碳检验。向碘的四氯化碳溶液中加入Na2SO3稀溶液,将I2还原,以回收四氯化碳。
①Na2SO3稀溶液与I2反应的离子方程式是____________________________________________。
②某学生设计回收四氯化碳的操作步骤为:
a.将碘的四氯化碳溶液置于分液漏斗中;
b.加入适量Na2SO3稀溶液;
c.分离出下层液体。
以上设计中遗漏的操作及上述步骤中的位置是_____________________________________________。
(3)已知:I2+2S2O32 - = 2I-+S4O62 -。某学生测定食用精制盐的碘含量,其步骤为:
a.准确称取w g食盐,加适量蒸馏水使其完全溶解;
b.用稀硫酸酸化所得溶液,加入足量KI溶液,使KIO3与KI反应完全;
c.以淀粉溶液为指示剂,逐滴加入物质的量浓度为2.0×10-3 mol/L的Na2S2O3溶液10.0 mL,恰好反应完全。
①判断c中反应恰好完全依据的现象是______________________________________________。
②b中反应所产生的I2的物质的量是________mol。
③根据以上实验和包装袋说明,所测精制盐的碘含量是(以含w的代数式表示)_________________mg/kg。
[答案](1)1、5、3、3、3、3。
(2)①I2+SO32 -+H2O = 2I-+SO42 -+2H+;②在步骤b后,增加操作:将分液漏斗充分振荡后静置。
(3)①溶液由蓝色恰好变为无色。 ②1.0×10-5。
[提示](3)③食盐中碘以KIO3形式存在,b中反应所产生的I2中只有1/5是来自于KIO3。要注意单位是mg/kg。
26.(2007年高考理综四川卷,卤素)(18分)在实验室里可用下图所示装置制取氯酸钾、次氯酸钠和探究氯水的性质。
图中:①为氯气发生装置;②的试管里盛有15 mL 30% KOH溶液,并置于水浴中;③的试管里盛有15 mL 8% NaOH溶液,并置于冰水浴中;④的试管里加有紫色石蕊试液;⑤为尾气吸收装置。
请填写下列空白:
(1)制取氯气时,在烧瓶里加入一定量的二氧化锰,通过_____________(填写仪器名称)向烧瓶中加入适量的浓盐酸。实验时为了除去氯气中的氯化氢气体,可在①与②之间安装盛有_______(填写下列编号字母)的净化装置。
(A)碱石灰 (B)饱和食盐水 (C)浓硫酸 (D)饱和碳酸氢钠溶液
(2)比较制取氯酸钾和次氯酸钠的条件,二者的差异是:________________________________________________。
反应完毕经冷却后,②的试管中有大量晶体析出。下图中符合该晶体溶解度曲线的是_______(填写编号字母);从②的试管中分离出该晶体的方法是__________(填写实验操作名称)。
 (3)本实验中制取次氯酸钠的离子方程式是______________________________________。
(3)本实验中制取次氯酸钠的离子方程式是______________________________________。
(4)实验中可观察到④的试管里溶液的颜色发生了如下变化,请填写下表中的空白:
|
实验现象 |
原因 |
|
溶液最初从紫色逐渐变为_______色 |
氯气与水反应生成的H+使石蕊变色 |
|
随后溶液逐渐变为无色 |
_______________________________ |
|
然后溶液从无色逐渐变为_______色 |
_______________________________ |
[答案](1)分液漏斗;B。 (2)碱溶液(或反应物)的浓度不同,反应温度不同; M; 过滤。
(3)Cl2+2OH- = ClO-+Cl-+H2O。 (4)
|
红 |
|
|
|
氯气与水反应生成HClO将石蕊氧化为无色物质 |
|
黄绿 |
继续通入的氯气溶于水使溶液呈黄绿色 |
- 上一篇:07年高考化学试题分类汇编——物质的量
- 下一篇:化学实验基本操作若干知识点归纳